1. 塩酸の正体と「電離」のメカニズムを再定義する

理科の学習において、現象の背後にあるミクロな動きを理解することは極めて重要です。
塩酸とは、単なる液体ではなく、気体の塩化水素 (HCl) が水に溶解した水溶液を指します。
この塩化水素は「電解質」としての性質を持ち、水中で陽イオンと陰イオンに分かれる電離という現象を起こします。
具体的には、化学式 HCl で表される塩化水素分子が、水の中で 水素イオン (H+) と 塩化物イオン (Cl-) に分かれます。
この際、前方に位置する水素が電子を失ってプラスの電気を帯び、後方の塩素が電子を受け取ってマイナスの電気を帯びるという原則を忘れてはいけません。
「塩化水素を水に溶かすと、水素イオンと塩化物イオンに電離する。この状態が塩酸である」
この電離状態こそが、その後の電気分解におけるすべての反応の起点となります。
電子の過不足が生まれることで、外部からの電気的な作用に対してイオンが能動的に動く準備が整うのです。
モデル図でイメージする際は、1対1で結びついていた原子が、電荷を持って離れ離れになる様子を思い浮かべてください。
重要な気づき: 電離は、電流を流す前から水溶液中で既に完了している現象です。
| 物質名 | 化学式 | 電離後の状態 | 電荷 |
|---|---|---|---|
| 塩化水素 | HCl | 水素イオン / 塩化物イオン | H+ (陽) / Cl- (陰) |
この基礎を疎かにすると、後の電極反応で「なぜイオンが移動するのか」という論理が破綻してしまいます。
物質の構成要素と電荷の関係を正しく把握することが、化学分野攻略の第一歩となります。
2. 電極で起きる電子の受け渡しと「酸化・還元」の萌芽

装置に電圧をかけると、水溶液中のイオンは「プラスとマイナスは引き合う」という物理法則に従って移動を開始します。
ここで注目すべきは、陽極 (プラス極) と 陰極 (マイナス極) で行われる、極めてシステマチックな電子の交換作業です。
まず、マイナスの電気を帯びた塩化物イオン (Cl-) は、プラス極である陽極に引き寄せられます。
陽極に到達した塩化物イオンは、余分に持っていた電子を電極へと渡します。
電子を失うことで、イオンは元の塩素原子へと戻りますが、原子単体では不安定なため、2つの原子が結合して 塩素分子 (Cl2) となり、気体として発生します。
鍵: 陽極では「電子を捨てる」反応が起き、塩素ガスが発生する。
一方、陽極で放出された電子は導線を通って陰極へと移動します。
この電子を受け取りに行くのが、プラスの電気を帯びた水素イオン (H+) です。
陰極で電子を1つずつ受け取った水素イオンは、水素原子となり、さらに2つが合体して 水素分子 (H2) として放出されます。
- 塩化物イオン:陽極へ移動 → 電子を渡す → 塩素 (Cl2) 発生
- 水素イオン:陰極へ移動 → 電子を受け取る → 水素 (H2) 発生
この電子の受け渡しこそが電気分解の本質です。
目に見えない極微の世界で、電子という「バトン」が受け渡されることで、化合物が元の元素へと分解されていくプロセスは、まさに化学の醍醐味と言えるでしょう。
ゴール: どちらの極から何の気体が出るか、その理由をイオンの電荷から説明できるようにすること。
3. 化学反応式とイオンモデルの統合的理解
理論を学んだ後は、それを数式化するプロセス、すなわち化学反応式の作成へと進みます。
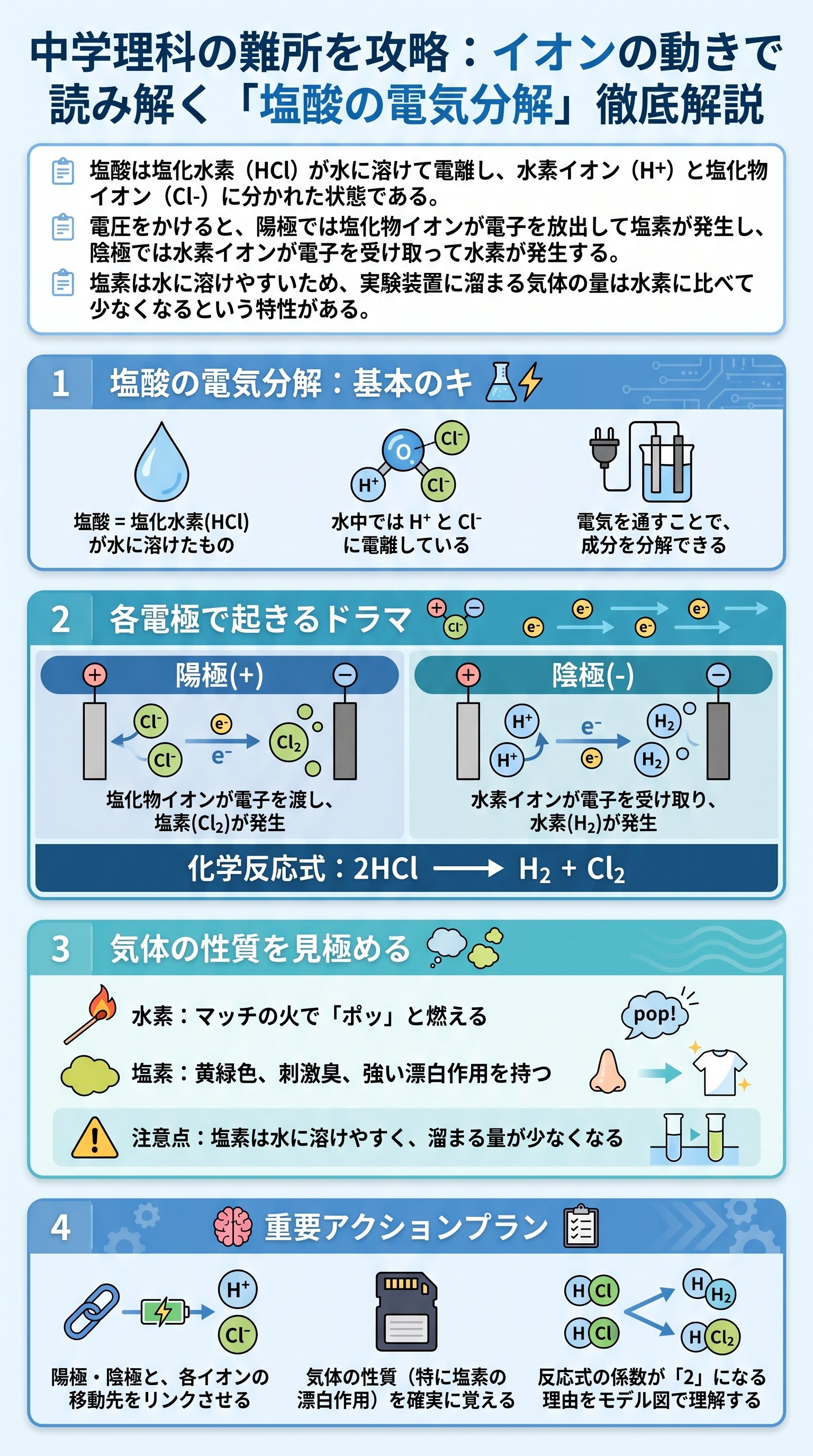
塩酸の電気分解における最終的な反応式は、2HCl → H2 + Cl2 と定義されます。