水素(Hydrogen)は、原子番号1番、陽子1個と電子1個で構成される最もシンプルな元素です。
しかし、そのシンプルさとは裏腹に、物理学や化学の根幹を成す極めて奥深い対象です。
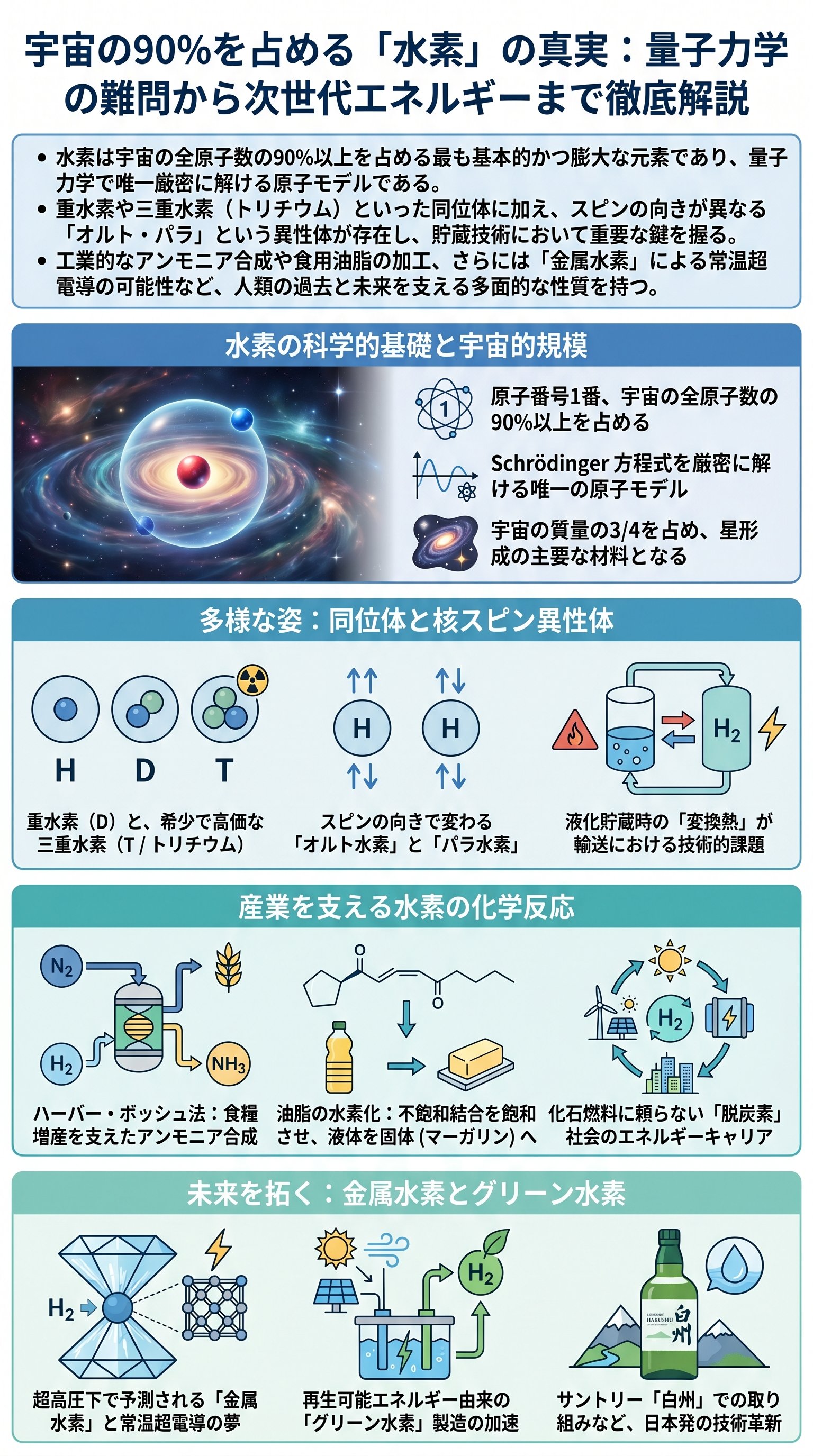
大学の理系学部で学ぶ量子力学では、Erwin Schrödinger (エルヴィン・シュレーディンガー) 方程式を用いて水素原子のエネルギー状態を計算しますが、これは厳密な解析解が得られる唯一の原子モデルとして知られています。
一方で、電子が2個以上になるだけで計算は一気に複雑化し、近似なしでは解けなくなります。
水素は、科学者がミクロの世界を理解するための「唯一の羅針盤」とも言える存在なのです。
宇宙全体を見渡せば、水素は質量の約3/4、原子数では実に90%以上を占める支配的な元素です。
宇宙誕生から約38万年後の「宇宙の晴れ上がり」の時期に形成され、今なお星々の主成分として存在しています。
地球上では、H2(水素分子)という気体の形ではほとんど存在せず、多くは水(H2O)や有機化合物の構成要素として留まっています。
私たちがエネルギーとして水素を利用するためには、これらの化合物から水素を「取り出す」プロセスが必要不可欠となります。
水素には性質の異なる「同位体」が存在します。

一般的な軽水素のほかに、中性子を1個持つ重水素(Deuterium / デューテリウム)と、2個持つ三重水素(Tritium / トリチウム)があります。
Deuterium は1934年にノーベル化学賞の対象となった発見であり、重水としての利用も研究されています。
一方、Tritium は放射性同位体であり、核融合発電の燃料として期待されていますが、その希少性から1gあたり約380万円もの高値で取引されることもあります。
これらは原子核の構成がわずかに異なるだけで、物理的・化学的に特異な挙動を示します。
また、水素分子(H2)には「オルト水素」と「パラ水素」という、原子核の回転(スピン)の向きが異なる2種類の異性体が存在します。
常温ではオルトとパラが3:1の割合で混在していますが、極低温で液化させるとエネルギー的に安定なパラ水素へとゆっくり変化します。
この変化の際に「変換熱」が発生するため、せっかく冷却して液化した水素が再び蒸発してしまうという工業的な課題が生じます。
水素を効率的に輸送・貯蔵するためには、このミクロなスピンの性質まで制御する必要があるのです。
水素の工業的利用は多岐にわたります。
最も有名なのは Fritz Haber (フリッツ・ハーバー) と Carl Bosch (カール・ボッシュ) が開発した「ハーバー・ボッシュ法」によるアンモニア合成です。

空気中の窒素と水素を反応させて肥料を作るこの技術は、「空気からパンを作る」と称され、爆発的な人口増加を支えました。
また、植物油に水素を添加(水素化)することで、液体の油を固体のマーガリンに変える技術も、分子の二重結合を単結合に変えて分子間力を強めるという化学的特性を利用したものです。
さらに未来の技術として注目されているのが「金属水素」です。
水素を超高圧(数百万気圧)の環境下に置くと、電子が特定の原子に縛られず自由に動き回る金属状態になると理論的に予測されています。
この金属水素は、常温付近で電気抵抗がゼロになる「常温超電導」を実現する有力候補とされています。
もし実現すれば、送電ロスをゼロにし、エネルギー革命を引き起こす「物理学の聖杯」となるでしょう。
1766年に Henry Cavendish (ヘンリー・キャベンディッシュ) によって発見された水素は、今や地球規模のサステナビリティを担う主役へと進化を遂げようとしています。
現在、サントリーグループが取り組む「グリーン水素パークー白州ー」のように、水を電気分解して水素を作る「水から生まれて、水に還る」エネルギーサイクルが始動しています。
CO2を排出しないクリーンなエネルギー源として、また産業構造を根本から変える素材として、水素の重要性は高まる一方です。
基礎科学から最先端の工業応用まで、水素という最も身近で最も奥深い元素を理解することは、これからのビジネスやテクノロジーを占う上で避けては通れない道と言えるでしょう。