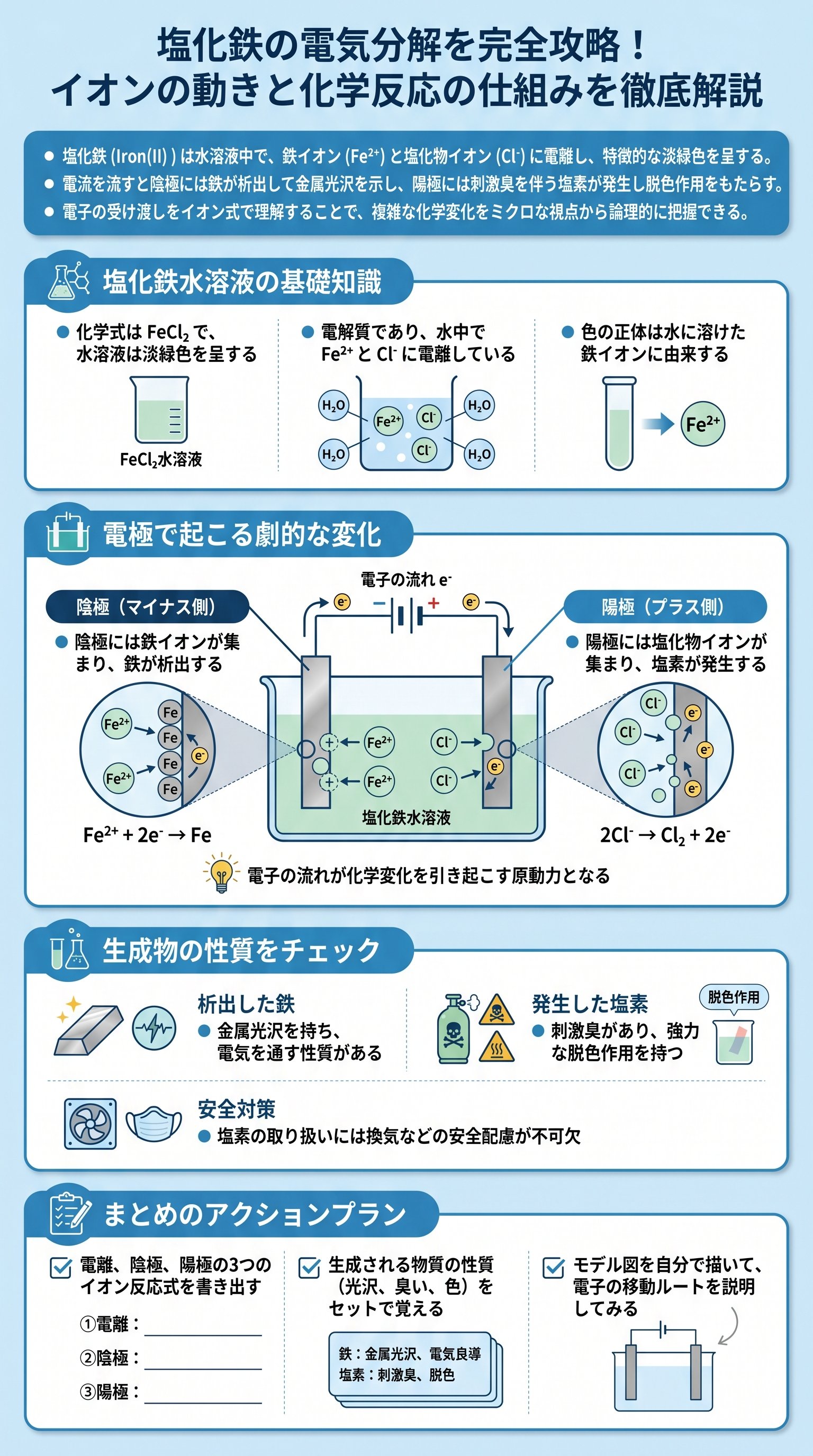
塩化鉄水溶液の構造:電離のメカニズム

理科の学習において「電気分解」は、物質の正体を知るための極めて重要なプロセスです。
今回扱う塩化鉄 (Iron(II) Chloride) は、化学式 `FeCl2` で表される物質であり、これを水に溶かした塩化鉄水溶液は、特有の淡緑色(薄い緑色)をしています。
この色の正体を知るためには、水溶液中で物質がどのような状態で存在しているかを理解しなければなりません。
重要な気づき: 物質が水に溶けて電流を流す状態になるものを「電解質」と呼び、塩化鉄はその代表例です。
塩化鉄は水に溶けると、鉄イオン (Fe2+) と塩化物イオン (Cl-) に分かれます。
これを「電離」と呼びます。
鉄の原子1個に対して塩素の原子が2個結びついているため、電離した際も鉄イオン1個に対して塩化物イオンが2個生じるのがポイントです。
この比率が、後の化学反応式のバランスを考える上で非常に重要になってきます。
鉄イオンはプラスの電気を帯びた「陽イオン」であり、塩化物イオンはマイナスの電気を帯びた「陰イオン」です。
イオンの電荷を正しく把握することが電気分解理解の第一歩といえるでしょう。
塩化物イオンがマイナス1の電気を2つ持っているため、全体のバランスを取るために鉄はプラス2の電気を帯びているのです。
このように、水溶液中では目に見えないミクロな粒子が電気的なバランスを保ちながら浮遊しています。
- 塩化鉄の化学式:`FeCl2`
- 鉄イオン:`Fe2+` (陽イオン)
- 塩化物イオン:`Cl-` (陰イオン)
- 水溶液の色:淡緑色(黄緑色に近い薄い緑)
電子の旅:電極における化学反応

水溶液に電極を差し込み、電源装置をつなぐことでドラマチックな変化が始まります。
電源のプラス極につながれた電極を「陽極」、マイナス極につながれた電極を「陰極」と呼びます。
電流を流すと、水溶液中のイオンは電気的な引力によってそれぞれの電極へと引き寄せられていきます。
マイナスの電気を持つ塩化物イオンは陽極へ、プラスの電気を持つ鉄イオンは陰極へと移動を開始するのです。
鍵: イオンが電極に引き寄せられるのは、異なる符号の電気同士が引き合うという物理原則に基づいています。
電極にたどり着いたイオンたちは、そこで「電子の受け渡し」を行います。
この電子の移動こそが電気分解の本質です。
陽極に到達した塩化物イオンは、余分に持っている電子を電極に捨てます。
捨てられた電子は導線を通って電源を経由し、反対側の陰極へと送り込まれます。
このように、回路全体を電子が循環することで電流が流れる仕組みになっています。
一方、陰極に到達した鉄イオンは、送られてきた電子を受け取ります。
プラスの電気を帯びていた鉄イオンが電子(マイナスの電気)を受け取ることで、電気的に中性な「鉄の原子」へと戻るのです。
このプロセスを経て、水溶液中に溶けていた成分が目に見える形の物質として取り出されることになります。
電子の授受を理解すれば、化学反応の全容が見えてくるはずです。
| 電極 | 引き寄せられるイオン | 電子の動き | 起こる変化 |
|---|---|---|---|
| 陽極 | 塩化物イオン (Cl-) | 電子を捨てる | 塩素ガスが発生 |
| 陰極 | 鉄イオン (Fe2+) | 電子を受け取る | 鉄が析出 |
陰極に現れる真実:鉄の析出と性質
陰極で起こる変化を詳しく観察してみましょう。
鉄イオンが電子を受け取ると、電極の表面に鉄 (Iron) が付着し始めます。